Was Vögel vom Menschen unterscheidet
H5N1, H7N9, H5N6 wann immer sich plötzlich Menschen mit einem Vogelgrippevirus anstecken, muss die Weltgesundheitsorganisation WHO das Risiko bewerten: Sind das die ersten Anzeichen einer Pandemie? Oder bleibt es bei einigen Dutzend, vielleicht auch Hunderten Fällen, die nur durch engen Kontakt mit infiziertem Geflügel entstehen? Forscher um Professor Matthias Selbach vom Max-Delbrück-Centrum für Molekulare Medizin haben nun einen weiteren Puzzlestein gefunden, der bei dieser ersten Einschätzung wichtig sein könnte.
- Veröffentlicht am
Vogelgrippeviren des Typs Influenza A können demnach infizierte menschliche Zellen nicht so gut in Virenfabriken verwandeln, sie produzieren dort nämlich nicht genug von ihrem Matrix-Protein M1. Das jedoch brauchen die Viren, um ihr vielfach kopiertes Erbgut wieder aus dem Zellkern heraus zu schleusen eine Voraussetzung, um neue Viren zu bauen, berichten die Forscher im Fachblatt Nature Communications.
Warum sind menschliche Zellen schlechte Virenfabriken für Vogelgrippeviren?
Hämagglutinin von Mensch und Vogel haben zum Beispiel einen leicht unterschiedlichen chemischen Aufbau. So fälltes einem Vogelgrippevirus schwerer, in eine menschliche Zelle einzudringen als in die eines Vogels, sagt Selbach.Welche weiteren natürlichen Speziesbarrieren es bei Grippeviren gibt, war die zentrale Fragestellung des Doktoranden Boris Bogdanow in seiner Arbeitsgruppe, dem Erstautor der aktuellen Studie. Das Vogelgrippevirus und das menschliche Virus unterschieden auf den ersten Blick wenig in der Proteinproduktion, was uns doch ziemlich überraschte.
Der Teufel steckt im Detail
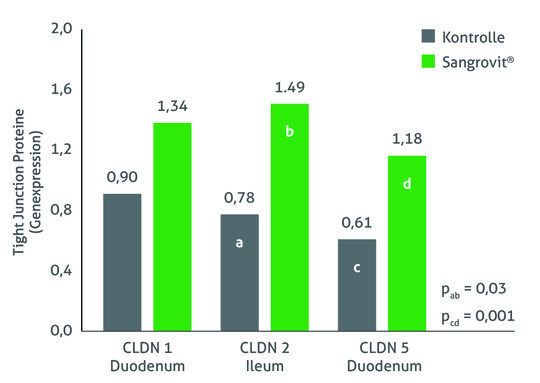
Und so griff Bogdanow zu tiefgreifenderen Analysen, um sich die Proteinverteilung genauer anzusehen. Dabei stieß er auf das Matrix-Protein M1: Es wurde in den Lungenzellen, die vom humanen Virus infiziert waren, in weit größeren Mengen hergestellt. Das M1-Protein ist unter anderem dafür zuständig, die vervielfältigte Viren-RNA wieder aus dem Zellkern der infizierten Zellen heraus zu schleusen, um dann mit anderen neuproduzierten Virenproteinen zu den Nachkommen der Grippeviren zusammengebaut zu werden. Könnte es also sein, dass die Viren-RNA der Vogelgrippeviren in menschlichen Zellen quasi im Zellkern gefangen bleibt, weil zu wenig M1-Protein vorhanden ist?
Ein weiterer Puzzlestein
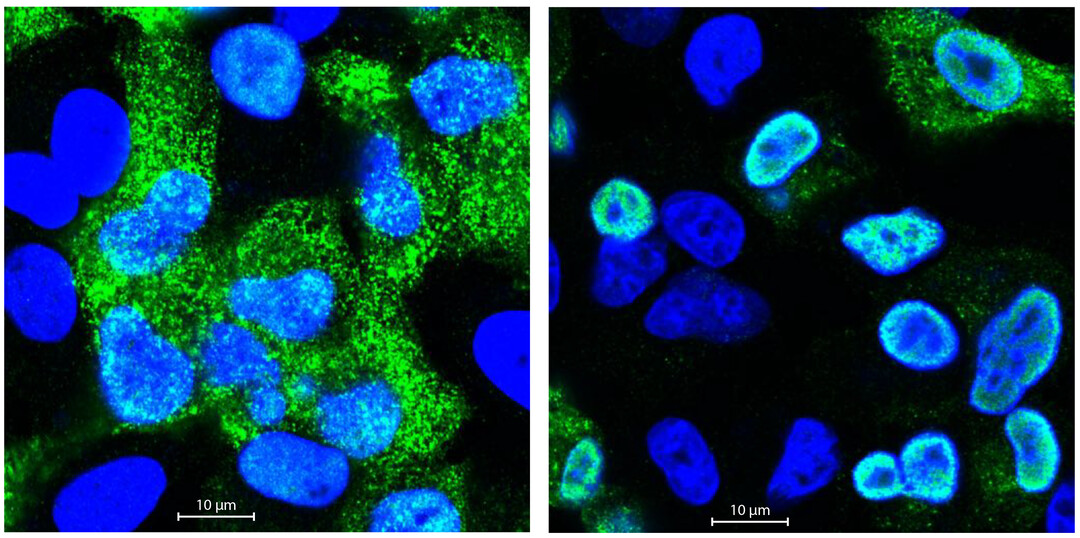
Fluoreszenzmikroskopische Untersuchungen bestätigten den Verdacht: Das Erbgut des Vogelgrippevirus schaffte es viel schlechter, aus dem Zellkern auszubrechen als die RNA des humanen Grippevirus. Aber warum? Gemeinsam mit der Sequenzierplattform des MDC und Professorin Irmtraud Meyer entdeckten sie einen kleinen Abschnitt in der Viren-RNA des Vogelgrippevirus, der alternatives Spleißen beeinflusst. Wir nennen das ein cis-regulatorisches Element, sagt Bogdanow. Alternatives Spleißen regelt nämlich, welche Proteine schlussendlich aus einem Gen gemacht werden, denn viele Gene kodieren für mehr als ein Protein. Wenn menschliche Zellen von Vogelgrippe befallen werden, sorgt dieses Element dafür, dass mehr M2- statt M1-Protein hergestellt wird.
Um die Relevanz dieses Ergebnisses abzuschätzen, übertrugen die Forscher um Professor Thorsten Wolff vom Robert Koch-Institut das cis-regulatorische Element vom Vogel- auf das Menschenvirus. Tatsächlich konnte sich dadurch das menschliche Grippevirus nun schlechter in menschlichen Lungenzellen vermehren. Einen ähnlichenVersuch machte das Team um Selbach sogar mit Viren der Spanischen Grippe, deren Erbmaterial in den Neunziger Jahren aus Gräbern im Permafrostboden Alaskas isoliert wurde. Sie verwendeten für dieses Zellkultur-Experiment allerdings nur einen kleinen Teil der Viren-RNA und nicht das gesamte Virus. Dennoch konnten sie damit ihre These zum cis-regulatorischen Element auch für dieses Virus bestätigen.
Wie pathogen ein Vogelgrippevirus ist und ob potenziell eine Pandemie droht, hängt natürlich von vielen Faktoren ab, sagt Selbach. Eine Studie in Zellkulturen kann das nicht alles abdecken. Dennoch kann es sinnvoll sein, in Zukunft eineAnalyse dieses RNA-Abschnitts in die Risikobewertung von Vogelgrippeviren einzubeziehen.